UNA ACTIVIDAD AUXILIAR DE CIENCIA y DEPORTE
por IRENE WAIS
Mucho es lo que ignoramos en materia de insectos acuáticos. Cubrir ese “bache” interesa a la biología ya la pesca. De hecho, saber acerca de especies y ciclos de vida resulta clave para “mosqueros”
Por eso esta invitación a coleccionarlos.
Para coleccionar ninfas de insectos acuáticos (y otros invertebrados), las artes de muestreo ideadas por el hombre son tan múltiples como los objetivos que lo han llevado a juntar estos animales a lo largo de varios siglos. La búsqueda del conocimiento e interpretación de su morfología, anatomía y distribución, en las primeras etapas de la entomología; posteriormente el estudio de la fisiología, desarrollo y comportamiento de esos insectos, y la comprensión de su bioquímica celular, los mecanismos intervinientes aún a nivel molecular y las bases de la moderna gen ética, han conducido a la elaboración de programas de muestreo que involucran cuidadosas y sofisticadas técnicas de recolección, cuya variedad responde a los distintos objetivos propuestos.
Sin embargo, a fin de lograr una simple serie cualitativa y representativa de insectos y otros invertebrados acuáticos, para la confección de un catálogo de “moscas”, la técnica a emplear es relativamente sencilla y puede ser llevada a cabo por un pescador aún no experimentado.
La metodología es la que se describe a continuación, a través de diez pautas básicas.
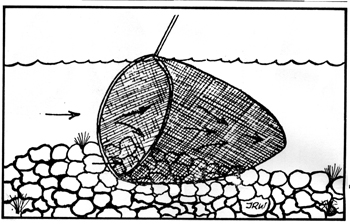
1) Colocar una red de malla de no más de 4 mm2 de abertura (si tiene menos, mejor aún), de tal manera que quede “encajada” entre los cantos rodados del fondo de los arroyos y ríos trucheros. Tratar en lo posible de hacer esta operación tanto en los rápidos como en las zonas remansadas, por separado y especificando en las referencias a cuál de estos dos lugares corresponde cada muestra.
2) Remover luego las piedras, para que los organismos acuáticos que se encuentran entre ellas pasen al fondo de la red con la sola acción de la corriente, impulsados por ésta (ver figura). Evitar el reflujo de la red con la consiguiente pérdida de material biológico.
3) Verter agua del arroyo en una bandeja blanca o, en su defecto, un plato -preferentemente de color muy claro, para observar los organismos acuáticos-, hasta llegar a la mitad de la altura de ese recipiente.
A continuación “lavar” muy bien el contenido de la red recientemente sacada del agua, dando vuelta la malla y cuidando de no “perder” ningún invertebrado.
4) Echar en un frasco de boca ancha y de tapa involcable, si es doble ya rosca mejor aún. De sobrar líquido, “colar” el contenido de la bandeja o plato con una sección de la red. Introducir todo animal que hubiere quedado adherido al recipiente plano, ayudándose con un pincel o pinza, y procurando no apretar el material biológico. Agregar unas pocas gotas de formol puro (que resulte una solución final del 3-4% de formol, ni más, ni menos) o bien colocar a cambio 7 partes de alcohol común de enfermería por cada 33 equivalentes de agua (logrando así una solución de alcohol de 70″, aproximadamente).
5) En el caso de las muestras de los rápidos, poner especial cuidado en observar las piedras, porqué hay numerosos insectos acuáticos con dispositivos de “agarre” o de “enganche”, que no van a pasar al interior de la red excepto que se los extraiga raspando las piedras con un cuchillo o espátula. Tener particular cautela de no dañar el animalito, ya que a veces las estructuras estropeadas dan información taxonómica sobre la especie de que se trata.
6) Colocar una etiqueta de papel vegetal (tipo “de plano”, más bien grueso, para que perdure) dentro del frasco con cada muestra, en la cual previamente se anotó el lugar (cuanto más preciso, mejor): río, localidad, provincia. Si es un arroyo pequeño, sin nombre, dar alguna referencia cercana. Por ejemplo: “A 2 kilómetros aguas arriba de la desembocadura en el lago Huechulafquen en Puerto Canoa”, o ” A 200 metros aguas abajo del puesto de Gendarmería”, etc. Se aconseja la máxima precisión posible (”Río Collón Cura, bajo puente de cruce de la ruta 237″). Agregar también fecha y nombre del colector.
7) Anotar todos estos datos en la etiqueta inmediatamente luego de tomada la muestra. No confíe en su memoria. Los frascos, luego de acumular varios, serán todos similares y puede confundir los lugares de muestreo. Dado que el papel vegetal debe introducirse dentro del líquido de los envases, deben hacerse las inscripciones con tinta china (con lapiceras de las del tipo que utilizan los arquitectos), insoluble en agua. De no contar con ésta, recurrir a un lápiz negro común de grafito, que no destiñe. No usar lápices de los de tipo acuarela.
8) No mezclar las muestras de los remansos con las de los rápidos; pero colocar todo lo que sale en las “redadas” efectuadas en el mismo lugar y localidad dentro de un único recipiente. Así, se puede poner la red varias veces en los rápidos para, por ejemplo, :1umentar la eficiencia de la recolección, y -siempre que esas muestras provengan todas de un solo lugar- pueden guardarse en el mismo frasco. La única precaución que se debe tomar es ir recogiendo las muestras siempre desde “aguas abajo” hacia “aguas arriba”; es decir, en sentido contrario a la corriente, para evitar pisar y perturbar el hábitat de lo que se muestreará luego.
9) Con frecuencia los adultos de las ninfas o larvas acuáticas se encuentran en las márgenes de los cursos de agua. Es importante también recogerlos, si es posible, ya que muchas veces ayudan a identificar a sus estados larvales.
10) No despreciar cursos de agua menores, por más insignificantes que parezcan, ya que los peces pueden incursionar en ellos para alimentarse. Ante la duda de si un grupo de piedritas es o no “basurita” del fondo solamente (o maderitas, ramitas, hojas pequeñas pegadas, etc.), recogerlo y guardarlo. No olvidar que pueden ser habitáculos de: “caddisflies”. Es muy importante no dejar de colocar la etiqueta. El material sin procedencia no tiene relevancia científica.
* Irene Rut Wais es bióloga del Museo Argentino de Ciencias Naturales “Bernardino Rivadavia” y del Instituto de Investigaci6n de las Ciencias Naturales. Actúa como asesora en la materia de nuestra revista, en cuyas páginas publica habitualmente.



Deja un comentario